一次性使用无菌注射针由针座、针管和保护罩组成,所用材料符合医疗要求。产品经环氧乙烷消毒。本品适用于皮内、皮下、肌肉、静脉注射或提取液体药物使用。注射针是医用接触类产品,所以需要严格检测,以下为您提供关于注射针检测以及注射针测试仪的知识 ~

注射针测试项目:
检测项目为外观、容量公差、尺寸、护套、针管外观、针管尺寸、针管长度、活塞组件、锥头、剩余容量、管体紧密度、滑动性能、pH值、易氧化物、环氧乙烷残留量、清洁度、色标、完整性、连接牢固度、光滑度、针座与护套配合度、针管润滑剂、针管清洁度、针管刚性等。
注射针测试标准:
JIS T3209-2011 无菌注射针
YY/T 0282-2009 注射针
GB 15811-2016 一次性使用无菌注射针
JIS T3305-2013 造影剂用注射针
JIS T6130-2013 一次性无菌牙科注射针
JIS T3306-2012 一次性使用神经兴奋阻滞注射针
JIS T3304-2012 一次性使用无菌硬脑膜外注射针
GB/T 12256-1990 注射针针管刚度试验方法
GB/T 1962.1-2001 注射器、注射针及其他医疗器械6%(鲁尔)圆锥接头 第1部分;通用要求
GB 15811-2001 一次性使用无菌注射针
GB/T 1962.2-2001 注射器、注射针及其他医疗器械6%(鲁尔)圆锥接头 第2部分;锁定接头
一次性使用无菌注射针GB 15811-2016(20180101)
《一次性使用无菌注射针》由中华人民共和国国家质量监督检验检疫总局、中国国家标准化管理委员会于2016年6月14日发布,自2018年1月1日实施。
·前 言
本标准的全部技术内容为强制性。本标准按照GB/T 1.1-2009给出的规则起草。本标准代替GB 15811-2001《一次性使用无菌注射针》,与GB 15811-2001相比较,主要技术变化如下:
——增加了第5章“材料”;
——增加了附录A注射针流量试验装置示意图;
——将针尖穿刺力要求以附录B(资料性附录)给出注射针针尖穿刺力要求及试验方法;
——删除了4.3.1针管刚性、4.3.2针管韧性和4.3.3针管耐腐蚀性条款;
——增加了初包装应使用纸塑透析包装材料的要求;
——修改了附录D检验规则,本标准使用重新起草法参考ISO7864:1993《一次性使用无菌皮下注射针》编制,与ISO7864:1993的一致性程度为非等效。
请注意本文件的某些内容可能涉及专利。本文件的发布机构不承担识别这些专利的责任。本标准由国家食品药品监督管理总局提出,本标准由全国医用注射器(针标准化技术委员会(SAC/TC95)归口。本标准起草单位:浙江康德莱医疗器械股份有限公司、上海市医疗器械检测所。
本标准主要起草人:张洪辉、丁彪。本标准所代替标准的历次版本发布情况为:
——GB 15811-1987、GB 15811-1995、GB 15811-2001。
1范 围
本标准规定了针管公称外径为0.3mm-1.2mm的一次性使用无菌注射针(以下简称注射针)的要求,本标准规定的注射针是与GB 15810一次性使用无菌注射器配套使用,也适合于其他相适宜的注射器具配套使用,作为对人体皮内、皮下、肌肉、静脉等注射药液用。本标准不适用于一次性使用牙科注射针。非灭菌状态供一次性使用无菌注射器配套的一次性使用注射针可参照本标准。
2规范性引用文件
下列文件对于本文件的应用是必不可少的。凡是注日期的引用文件,仅注日期的版本适用于本文件,凡是不注日期的引用文件,其最新版本(包括所有的修改单)适用于本文件。
GB/T 1962.1-2015注射器、注射针和其他医疗器械6%(鲁尔)圆链接头第1部分:通用要求(ISO594-1:1986,IDT)
GB/T 1962.2-2001注射器、注射针和其他医疗器械6%(鲁尔)圆锥接头第2部分:锁定接头(ISO594-2:1998,IDT)
GB/T 6682分析实验室用水规格和试验方法
GB/T 6682-2008,ISO 3696:1987:MOD)
GB/T 14233.1-2008医用输液、输血、注射器具检验方法第1部分:化学分析方法
GB/T 14233.2-2005医用输液、输血、注射器具检验方法第2部分:生物学试验方法
GB 15810一次性使用无菌注射器
GB 15810-2001,QvISO7886-1:1993)GB/T 16886.1医疗器械生物学评价第1部分:风险管理过程中的评价与试验(GB/T 16886.1-2011,ISO 10993-1:2009,IDT)
GB/T 18457-2015制造医疗器械用不锈钢针管(ISO 9626:1991,MOD)
YY/T 0296一次性使用注射针识别色标(YY/T0296-2013,ISO 6009:1992,IDT)
YY/TO466.1医疗器械用于医疗器械标签、标记和提供信息的符号第1部分:通用要求(YY/T 0466.1-2009,ISO 15233-1:2007,IDT)
3结构型式与命名
3.1 注射针的结构型式,各部分的名称术语和针管长度L如图1所示。
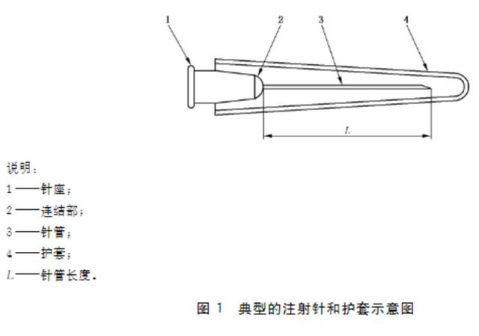
3.2 注射针针尖的几何图形及命名如图2所示。
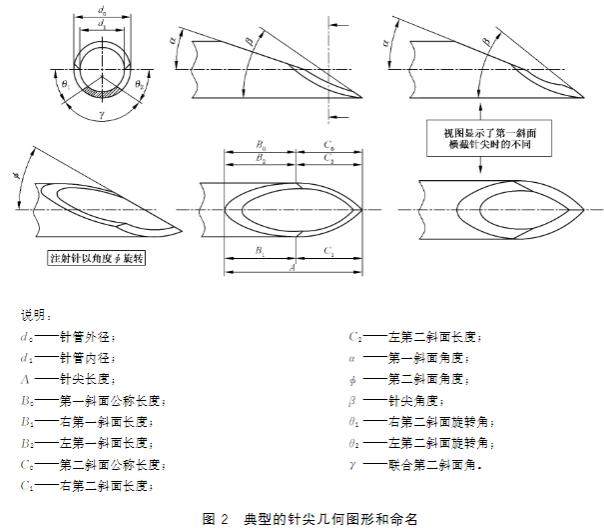
4标记示例
4.1 注射针产品的标记(规格)以针管公称外径、公称长度(图1中的I)、管壁类型和第一斜面角度(a)组成,外径和长度单位以“mm”表示,管壁类型以RW(正常壁)、TW(薄壁)或ETW(超薄壁)表示,第一斜面角度以LB(长斜面角)或SB(短斜面角)表示,
4.2 符合本标准要求的针管公称外径为0.7mm,长度(L)为30mm,管壁类型为薄壁,第一斜面角度为长斜面角的注射针标记为:0.7×30TWLB。
5材 料
5.1 制造注射针的针管应符合GB/T 18457-2015的要求。
注:针管的每一生产批应有刚性、韧性和耐腐蚀注信息.
5.2 制造针座的材料应满足第7章、第8章的要求。
6物理性能
6.1 清洁
在3001x~7001x照度下,用正常或矫正视力在不经放大条件下观察针管表面,和经2.5倍放大条件下观察针座表面应清洁,无异物。
6.2 色标
注射针应以针座和/或护套的颜色作为针管公称外径的标示,应符合YY/T0296的要求。
6.3 正直
目力观察针座与针管连接应正直,针管不应有明显的歪斜。
6.4 连接牢固度
针座与针管连接应牢固,将注射针针管固定在专用仪器上,以针座拨出方向,在表1规定的载荷下做无冲击的拉拔试验,两者不得松动或分离。
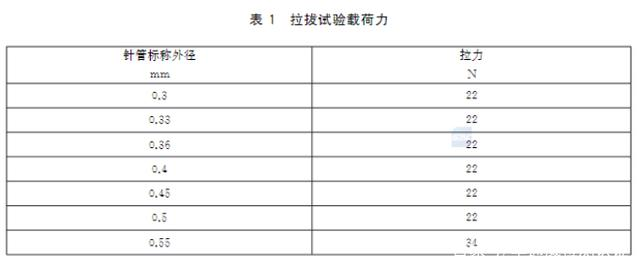
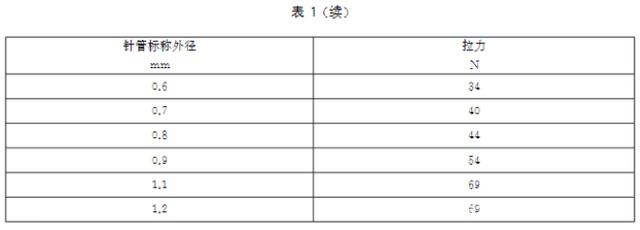
6.5 畅通
注射针的针孔应畅通:
a)按表2规定的通针可以自由通过;
b)或在不大于100kPa水压下,流量应不小于相同外径和长度的符合GB/T 18457-2015中规定的最小内径针管流量的80%,附录A给出了流量试验装置示意图。
6.6 针座与护套配合
注射针针座与护套配合应良好,护套不得自然脱落,将针座固定在专用仪器上,从保护套拉出方向,作无冲击拉拔,两者分离力应不大于15N。
6.7 针尖
在放大2.5倍条件下,用正常或矫正视力检查针尖应锋利,无毛边、毛刺和弯钩等缺陷。
注1:针尖的第一斜面角a(如图2所示)通常采用(11×2)。,通称长斜面:或采用(17×2)。,通称短斜面角;注2:附录B给出了针尖穿刺力试验和评价方法.
6.8 针管
6.8.1 针管表面使用润滑剂时,用正常或矫正到正常视力观察,针管内(针尖部分)外表面不应有可见的润滑剂积聚,
6.8.2 针管内应清洁:将甘油和酒精1:1混合均匀,然后用清洁的注射器将混合液5mL注射通过注射针,用正常或矫正到正常视力观察,流过针管内壁的混合液应无异物和脏物。
6.8.3 用通用量具检查,针管外径应符合GB/T 18457-2015中表1的规定,针管长度(图1中L)及偏差应符合表3的规定。
6.9 针座
6.9.1 用正常或矫正视力观察,针座应无明显毛边、毛刺、塑流及气泡等注塑缺陷。
6.9.2 针座为圆链接头式的,应符合GB/T 1962.1-2015的要求。GB/T 1962.1-2015给出了圆锥接头性能的试验方法。针座为锁紧接头式的,应符合GB/T 1962.2-2001的要求。GB/T 1962.2-2001给出了锁紧接头性能的试验方法。
7化学性能
7.1 检验液制备
将25支拔去护套的注射针浸入250mL新制成的符合GB/T 6682中规定的3级水中,在37℃±1℃
下恒温1h,取出注射针获取检验液;同时按上述同样方法不放注射针制备空白对照液,
7.2 酸碱度
按GB/T 14233.1-2008规定的方法试验时,检验液与同批对照液的pH之差不得大于1。
7.3 重金属总含量(金属离子)
用原子吸收分光光度计法(AAS)或相当的方法进行测定时,检验液中钡、铬、铜、铅和锡的总含量应不超过5ug/mL,镉的含量应不超过0.1ug/mL,按GB/T 14233.1-2008中5.6.1规定的方法试验时,检验液呈现的颜色应不超过浓度为5ug/mL的标准对照液的颜色。
8生物性能
8.1 检验液制备
将25支拨去护套的注射针浸入250mL无菌、无热原的0.9%氯化钠溶液中,在37℃±1℃下恒温1h,取出注射针获取检验液,检验液的贮存不得超过2h,
8.2 无菌
每一经初包装的注射针应选择适宜的方法进行灭菌,应对灭菌过程进行确认和常规控制,以保证产品上的细菌存活概率小于10-6,灭菌过程的确认应形成文件。
注:GB/T 14233.2中规定了无菌试验方法,该方法适用于型式试验而不适用于出厂检验。适宜的灭菌和出厂无菌检验方法见参考文献中的GB 18279或GB 18280。
8.3 细菌内毒素
按GB/T 14233.2-2005方法试验时,细菌内毒素含量应小于20EU/支。
8.4 溶血
按GB/T 14233.2-2005方法试验时,注射针的溶血率应小于5%。
8.5 生物相容性
应按GB/T 16886.1的要求对注射针进行生物学评价,评价结果应表明无生物学危害。附录C给出了注射针生物学评价的基本要求。
9包 装
9.1 初包装
每一支注射针应封装在初包装中,此包装的材料和设计应确保其中的色标可见。
采用环氧乙烷灭菌时,注射器初包装应采用一面透析纸另一面塑材或全透析纸的包装材料,本标准鼓励采用透析效果更好的包装材料。包装材料不得对内装物产生有害影响,此包装的材料和设计应确保:
a)在干燥、清洁和充分通风的贮存条件下,能保证内装物无菌;
b)从包装物中取出时,内装物受污染的风险最小;
c)在正常搬动、运输和贮存期间,初包装对内装物应能充分的保护;
d)一旦打开,包装物不能轻易地重新密封,而且应有明显的被撕开的痕迹。
9.2 中包装
一件或一件以上的初包装:应装入一件中包装中。
在正常搬运、运输和贮存期间,中包装对内装物应能充分的保护。
9.3 大包装
一件或一件以上的中包装:应装入一大包装中。
在正常搬运、运输和贮存期间,大包装应能充分保护内装物。
一次性无菌注射针测试仪器是什么?
威夏科技 CL15811-T医用注射针刺穿力测试仪

仪器特征
采用可编程控制器、液晶屏、力值传感器、测力机构、传动装置、机载打印机等组成,中文菜单显示,人机对话设定各项参数自动运行测试。操作方便。实时显示刺穿力值测试的载荷力值,并可由打印机打印测试数据和刺穿力值。实时显示刺穿力和峰值数据,可显示zui大刺穿力及F0-F4五种峰值力,通过曲线可以直接判断不合格原因。
技术指标
操作界面:简体中文
公称规格:0.1~3.4mm;(所有规格)
测试范围:0.05~10.00N、精度:±0.001N;
移动速度:100mm/min;
(赠送)模拟皮肤:聚氨酯膜材料,
标准:符合GB/T15811-2016标准;
打印方式:每次可打印8次、13次或20次测试数据及平均挠度值和偏差值。
净 ???重:11kg
外形尺寸:400×290×240(mm)
电????源:AC220V,50Hz
整机功率:60W
设备应用:
CL15811-T医用注射针刺穿力测试仪主要用于测定医用注射针的针jian刺穿力的物理特性,是鉴定医用注射针针尖的重要手段之一。
威夏科技 CL15811-C医用注射针刺穿力测试仪

仪器特征
本设备是检验生产厂家产品性能的检测设备。由可编程控制器,触摸屏,力值传感器,传动装置,机载打印机等组成,提供中英文菜单显示,设定了人机对话各项参数自动运行测试模式。另增设生产单位,生产批次机打输入,使测试结果更加规范化标准化。信息安全方面采用三级密码,让信息安全可靠。测试操控范围包括:公称规格、管壁、打印设定、测试、上行、下行、时间、标定等功能设定。另搭配机载打印机,实时显示穿刺力曲线测试结果及zui大刺穿力数据。可现实F0到F5峰值数据。针对测试结果自动判断,不合格启动自动报警,并由打印机打印出测试数据及结果以供分析。是检验生产厂家产品能力的有效检测手段。
技术参数
操作界面:简体中文/英文
测试标准:GB/T 15811-2016 一次性使用无菌注射针
ISO 7864:2016 一次性使用无菌皮下注射针要求和试验方法
管 壁:正常壁、薄壁、超薄壁,超超薄壁四种任选;
公称规格:0.1~6.2mm(所有规格都可测试);
测量范围:0.001~10.0000N
精度:±0.0001N;
测试速度:100±0.1mm/min;(无极调速可任意设定)
模拟皮肤:聚氨酯膜材料 符合GB15811-2016标准
打印方式:每次可打印100次测试数据及平均值。
产品净重:12kg
外观尺寸:430×290×250(mm)
电 ???源:AC90V-240V/50Hz(自适应宽电压)
整机功率:70W
可编程控制器:PLC/ARM
触摸屏:7英寸K600+内核/点阵式65色800*480分辨率
传感器:高精度力值传感器
测力机构:内置
打印机:机载针式打印机
设备应用:
CL15811-C医用注射针刺穿力测试仪主要用于测定医用注射针针管针尖穿刺力性能的物理特性,是鉴定医用注射针的重要手段之一。
威夏科技 RX9626-T注射针管韧性测试仪

仪器特征
采用高亮度LED显示屏,采用PLC控制,弯曲角度、公称规格、支点与作用点间距、弯曲次数。由PLC可编程控制器设定程序,自动测试。
技术参数
操作页面:简体中文